МРНК-вакцына Pfizer супраць COVID зноў распаліла запал да выкарыстання рыбануклеінавай кіслаты (РНК) у якасці тэрапеўтычнай мішэні.Аднак таргетынг РНК з малымі малекуламі надзвычай складаны.
РНК мае толькі чатыры будаўнічыя блокі: адэнін (A), цытазін (C), гуанін (G) і урацыл (U), які замяняе тымін (T), знойдзены ў ДНК.Гэта робіць селектыўнасць лекаў амаль непераадольнай перашкодай.Наадварот, ёсць 22 прыродныя амінакіслоты, якія ўваходзяць у склад бялкоў, што тлумачыць, чаму большасць прэпаратаў, накіраваных на бялок, маюць адносна добрую селектыўнасць.
Будова і функцыі РНК
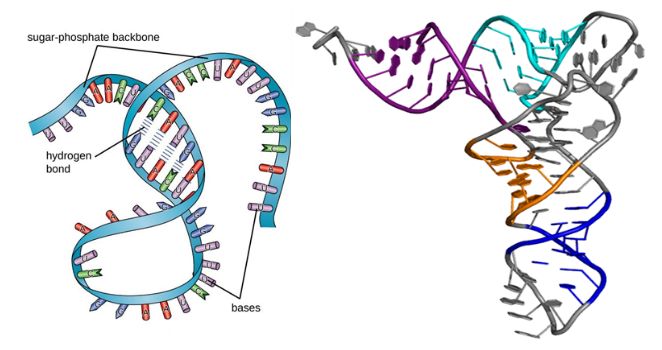
Як і вавёркі, малекулы РНК маюць другасную і троесную структуры, як паказана на малюнку ніжэй.Нягледзячы на тое, што яны з'яўляюцца адналанцуговымі макрамалекуламі, іх другасная структура набывае форму, калі спарванне асноў выклікае выпукласці, завесы і спіралі.Затым трохмернае згортванне прыводзіць да троеснай структуры РНК, якая важная для яе стабільнасці і функцыянавання.
Малюнак 1. Будова РНК
Ёсць тры тыпу РНК:
- Інфармацыйная РНК (мРНК)транскрыбуе генетычную інфармацыю з ДНК і пераносіцца ў выглядзе паслядоўнасці асноў на рыбасомы;л
- Рыбасомальная РНК (рРНК)з'яўляецца часткай арганэл, якія сінтэзуюць бялок, званых рыбасомамі, якія экспартуюцца ў цытаплазму і дапамагаюць трансляваць інфармацыю ў мРНК у вавёркі;
- Трансфер РНК (тРНК)з'яўляецца сувязным звяном паміж мРНК і ланцугом амінакіслот, з якіх складаецца бялок.
Нацэльванне РНК у якасці тэрапеўтычнай мішэні вельмі прывабнае.Было выяўлена, што толькі 1,5% нашага геному ў канчатковым выніку транслюецца ў бялок, у той час як 70%-90% транскрыбуецца ў РНК.Малекулы РНК з'яўляюцца найбольш важнымі для ўсіх жывых арганізмаў.Згодна з «цэнтральнай догмай» Фрэнсіса Крыка, самая важная роля РНК - трансляцыя генетычнай інфармацыі з ДНК у вавёркі.Акрамя таго, малекулы РНК выконваюць і іншыя функцыі, у тым ліку:
- Дзейнічаючы як адаптарныя малекулы ў сінтэзе бялку;л
- Служыць пасланнікам паміж ДНК і рыбасомай;л
- Яны з'яўляюцца носьбітамі генетычнай інфармацыі ва ўсіх жывых клетках;л
- Садзейнічанне выбару рыбасомамі правільных амінакіслот, неабходных для сінтэзу новых бялкоўу натуральных умовах.
Антыбіётыкі
Нягледзячы на тое, што былі адкрыты яшчэ ў 1940-х гадах, механізм дзеяння многіх антыбіётыкаў не быў высветлены да канца 1980-х гадоў.Выяўлена, што вялікая частка антыбіётыкаў дзейнічае, звязваючыся з бактэрыяльнымі рыбасомамі, каб прадухіліць іх выпрацоўку адпаведных бялкоў, тым самым забіваючы бактэрыі.
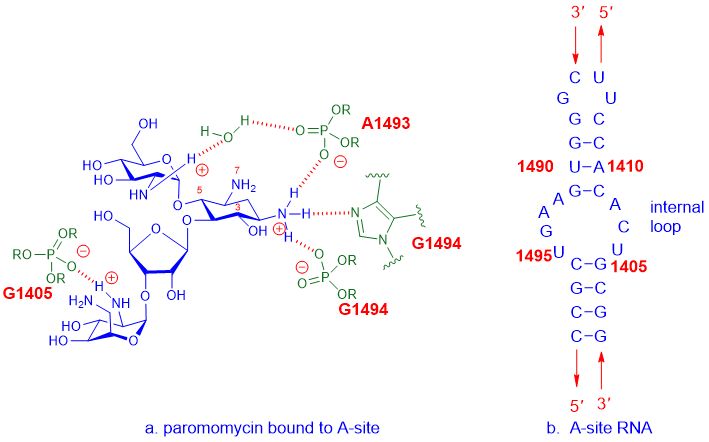
Напрыклад, амінагліказідныя антыбіётыкі звязваюцца з А-сайтам 16S рРНК, якая з'яўляецца часткай субадзінак 30S рыбасомы, а затым перашкаджаюць сінтэзу бялку, каб перашкаджаць росту бактэрый, што ў канчатковым выніку прыводзіць да гібелі клетак.А-сайт адносіцца да амінаацыльнага сайта, таксама вядомага як сайт акцэптара тРНК.Дэталёвае ўзаемадзеянне паміж амінагліказіднымі прэпаратамі, такімі якпаромомицин, і А-сайт зКішачная палачкаРНК паказана ніжэй.
Малюнак 2. Узаемадзеянне паромомицина і А-сайтаКішачная палачкаРНК
На жаль, многія інгібітары А-сайта, уключаючы амінагліказідныя прэпараты, маюць праблемы з бяспекай, такія як нефратаксічнасць, залежная ад дозы і спецыфічная незваротная ототоксичность.Гэтая таксічнасць з'яўляецца вынікам адсутнасці селектыўнасці амінагліказідных прэпаратаў для распазнання малых малекул РНК.
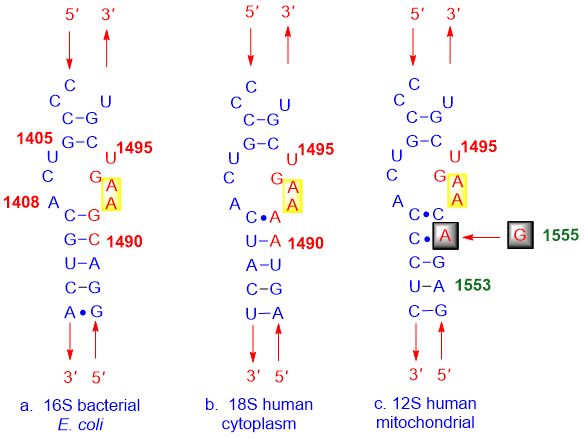
Як паказана на малюнку ніжэй: (а) структура бактэрый, (б) клеткавая мембрана чалавека і (в) мітахандрыяльны А-сайт чалавека вельмі падобныя, дзякуючы чаму інгібітары А-сайта звязваюцца з усімі імі.
Малюнак 3. Звязванне неселективного інгібітара А-сайта
Тэтрацыклінавай антыбіётыкі таксама інгібіруюць А-сайт рРНК.Яны селектыўна інгібіруюць сінтэз бактэрыяльнага бялку шляхам зварачальнага звязвання са спіральнай вобласцю (H34) субадзінак 30S, у комплексе з Mg2+.
З іншага боку, макролидные антыбіётыкі звязваюцца паблізу месца выхаду (E-сайт) бактэрыяльнага рыбасомнага тунэля для зараджаюцца пептыдаў (NPET) і часткова блакуюць яго, тым самым інгібіруючы сінтэз бактэрыяльнага бялку.Нарэшце, оксазолидинон антыбіётыкі, такія яклинезолид(Zyvox) звязваюцца з глыбокай шчылінай у бактэрыяльнай субадзінцы 50S рыбасомы, якая акружана нуклеатыдамі 23S рРНК.
Антысэнсавыя алігануклеатыды (ASO)
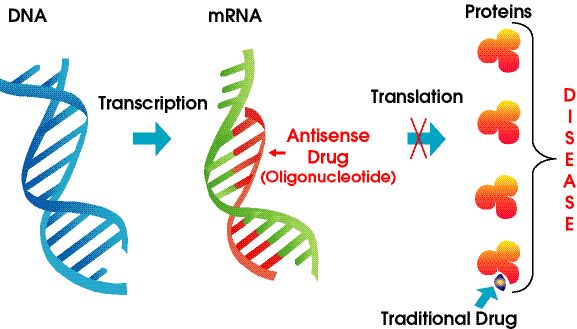
Антысэнсавыя прэпараты ўяўляюць сабой хімічна мадыфікаваныя палімеры нуклеінавых кіслот, якія нацэлены на РНК.Яны абапіраюцца на спарванне асноў Уотсана-Крыка для звязвання з мРНК-мішэнню, што прыводзіць да сайленсинга гена, стэрычнай блакады або змены сплайсінгу.ASO могуць узаемадзейнічаць з прэ-РНК у клеткавым ядры і спелымі мРНК у цытаплазме.Яны могуць нацэльвацца на экзоны, інтроны і нетрансляваныя вобласці (UTR).На сённяшні дзень больш за дзясятак прэпаратаў ASO былі адобраны FDA.
Малюнак 4. Антысэнс-тэхналогія
Прэпараты малой малекулы, накіраваныя на РНК
У 2015 г. Novartis паведаміла, што яны выявілі рэгулятар сплайсінгу SMN2 пад назвай Branaplam, які ўзмацняе асацыяцыю U1-pre-mRNA і ратуе мышэй SMA.
З іншага боку, Risdiplam (Evrysdi) PTC/Roche быў ухвалены FDA ў 2020 годзе для лячэння СМА.Як і Бранаплам, Рысдыплам таксама дзейнічае, рэгулюючы сплайсінг адпаведных генаў SMN2 для атрымання функцыянальных бялкоў SMN.
Дэградатары РНК
RBM расшыфроўваецца як бялок матыву, які звязвае РНК.Па сутнасці, індолсульфаніламід - гэта малекулярны клей.Ён выбарачна прыцягвае RBM39 да убиквитинлигазе CRL4-DCAF15 E3, спрыяючы полиубиквитинированию RBM39 і дэградацыі бялку.Генетычнае знясіленне або апасродкаваная сульфаніламідамі дэградацыя RBM39 выклікае значныя анамаліі сплайсінгу ў геноме, што ў канчатковым выніку прыводзіць да гібелі клетак.
РНК-PROTAC распрацаваны для дэградацыі РНК-звязваючых бялкоў (RBP).PROTAC выкарыстоўвае лінкер для злучэння ліганда E3-лігазы з лігандам РНК, які звязваецца з РНК і RBP.Паколькі RBP змяшчае структурныя дамены, якія могуць звязвацца са спецыфічнымі алігануклеатыднымі паслядоўнасцямі, RNA-PROTAC выкарыстоўвае алігануклеатыдную паслядоўнасць у якасці ліганда для цікавага бялку (POI).Канчатковым вынікам з'яўляецца дэградацыя RBP.
Нядаўна прафесар Мэцью Дысней з Інстытута акіянаграфіі Скрыпса вынайшаў РНКхімеры, накіраваныя на рыбануклеазу (RiboTACs).RiboTAC - гэта гетэрафункцыянальная малекула, якая злучае ліганд РНКазы L і ліганд РНК з дапамогай лінкера.Ён можа спецыфічна прыцягваць эндагенную РНКазу L да пэўных мішэняў РНК, а затым паспяхова ліквідаваць РНК з дапамогай клеткавага механізму распаду нуклеінавых кіслот (РНКазы L).
Калі даследчыкі даведаюцца больш пра ўзаемадзеянне паміж малымі малекуламі і РНК-мішэнямі, у будучыні з'явіцца больш лекаў, якія выкарыстоўваюць гэты метад.
Час публікацыі: 2 жніўня 2023 г